你体内的“铁”还稳定吗?一文解析铁调素与膜铁转运蛋白相互作用
2023-10-09 17:11 文章来源:
作者:周子琼
单位:阳江市中医医院
铁是所有生物体必需的微量营养元素,在维持生物体生存和功能所必需的代谢过程中占有重要地位,因为它参与血红蛋白合成、细胞呼吸的电子传递、DNA合成和其他重要的酶促反应。
生物有机体通过肠道铁的吸收,密切调节细胞内和细胞外的铁浓度和铁在器官和组织中分布维持稳态。
铁代谢障碍时会出现相应的临床疾病,例如铁缺乏会引起缺铁性贫血;铁过载会引起色素沉积症。
铁调素与铁转运蛋白
铁调素是介导细胞外铁浓度稳态的主要铁调节激素,通过调节十二指肠肠细胞、铁再循环巨噬细胞和铁储存肝细胞,将铁递送到血浆中,用于红细胞血红蛋白的合成以及组织消耗铁的其它用途。健康人体内铁调素的浓度大约为2-25nM。
该肽最初由肝脏合成为84个氨基酸的前铁调素原,通过信号肽酶和内切蛋白酶剪切加工,使其具有生物活性的25个氨基酸的多肽分泌到血浆中循环并在尿液中排泄。
铁转运蛋白是溶质载体家族的成员,系统地命名为SLC40A1,具有571个氨基酸,分子量约为65-70kD。唯一已知的细胞铁输出蛋白,由细胞质环连接的两个6-跨膜螺旋束组成,其中C-和N-末端均位于细胞质中,两个螺旋束包围一个空腔,铁被认为通过该空腔离开细胞。
铁调素与膜铁转运蛋白相互作用
铁的吸收和组织分布主要由铁调素与膜铁转运蛋白的相互作用控制。
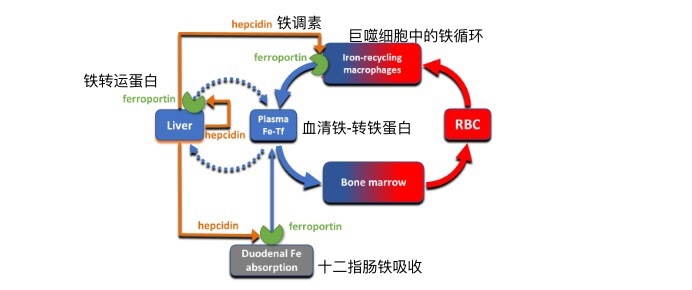
铁调素与膜铁转运蛋白的相互作用控制铁流入血浆
运铁蛋白从吸收膳食铁的十二指肠上皮细胞、脾和肝中的铁再循环巨噬细胞以及储存铁的肝细胞输出铁;铁调素浓度的增加抑制铁转运蛋白活性,导致血浆和细胞外液中铁的消耗。
铁调素合成减少或铁调素与膜铁转运蛋白结合被破坏可引起铁超负荷病症。
铁调素代谢
铁调素代谢机制主要有两种:
一是铁调素作为小分子肽可以通过肾小球的滤过膜,然后在近端小管被重吸收和降解。一小部分滤过的铁调素可在尿液中检测到;慢性肾衰竭患者的血清铁调素浓度非常高,血液透析后可减低,但是是短暂的,因为肝铁调素合成非常迅速,可以在数小时内恢复铁调素浓度。
二是高浓度铁转运蛋白的细胞对铁调素-铁转运蛋白复合物进行内吞作用与降解。
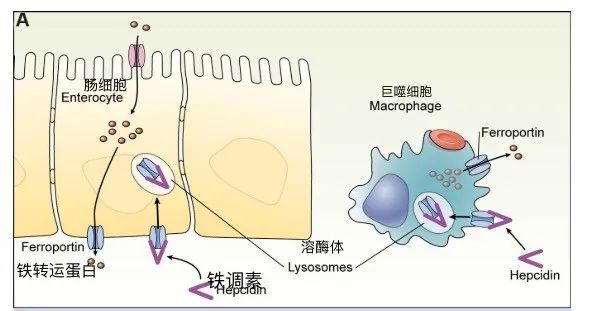
铁调素与血色病(A):描绘了铁调素的活性,显示膜铁转运蛋白作为肠细胞和巨噬细胞上的靶标。铁调素与膜铁转运蛋白结合,触发其内化和降解。
铁调素的临床运用价值
铁调素作为铁负调节激素,当个体铁充足时,铁调素水平高,从而限制铁吸收;当个体铁缺乏时,铁调素水平低,从而调节铁吸收和释放。
慢性病贫血(也称为炎症性贫血)
是一种获得性铁稳态紊乱,主要通过细胞因子白细胞介素-6(IL-6)的作用诱导铁调素上调,抑制细胞内铁向血浆释放,并导致肠铁吸收和铁再循环中断,从而限制铁对入侵微生物的可用性。
这种情况也可能与恶性肿瘤、器官衰竭、创伤或其他炎症原因有关。贫血通常为轻度至中度,红细胞可能不显示任何缺铁的标志。但潜在的铁病因是显而易见的,并且当铁-转铁蛋白可用时,红细胞前体反应非常迅速。
血色病(一种遗传性铁超载疾病)
1865年,Trousseau将血色素沉着症描述为“青铜色糖尿病”, 是最早发现与染色体位置相关的遗传病之一。铁调素缺乏是大多数遗传性血色素中铁超负荷的原因,肠铁吸收和巨噬细胞铁释放未得到适当控制,导致铁过载、血清铁增加以及肝脏、心脏和内分泌组织中的铁沉积。
血色病的分子发病机制可分为3类(图2B)。首先,铁调素基因本身(称为HAMP)的突变通过阻止功能性铁调素蛋白的产生而引起血色素沉着症。其次,编码HFE(HFE)、TFR2(TFR2)和血幼素(HFE2)的基因突变使上调铁调素表达的信号传导途径失活。最后,编码膜铁转运蛋白的基因突变可通过使转运蛋白对铁调素调节不敏感,从而引起血色素沉着症。
妊娠期间
为了维持适当的循环和孕妇的器官以及胎盘氧气的输送,铁调素浓度的下降使孕妇能吸收更多的铁,以用于自身血红蛋白合成以及胎儿的生长。
大多数缺铁病例是后天性的
由失血(如肠道寄生虫病)、膳食铁摄入不足或两者兼而有之所致。在缺铁期间或出血后,它将体内铁的需求传达给产生铁调素的肝细胞,使铁调素下调,允许铁通过膜铁转运蛋白递送至血浆。
慢性肾性贫血患者
因清除率降低及炎症诱导作用,使铁调素处于高水平,引起铁转运障碍。
幽门螺杆菌感染
最近,人们重新发现,幽门螺杆菌感染即使在没有显着出血的情况下,仍可导致严重的缺铁性贫血,并且口服铁剂治疗反应差。这种疾病通常见于年轻女性,与胃萎缩有关,并可能与其他自身免疫现象有关。
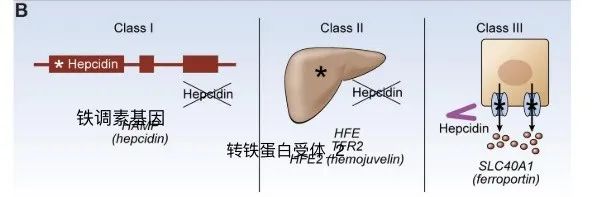
(B)血色素沉着症病症的分子发病机制可分为3类,均影响铁调素/膜铁转运蛋白调节轴:I类,铁调素基因(HAMP)中的缺陷阻止功能性铁调素的产生;II类,HFE、TFR2或HFE2基因的缺陷阻止肝脏中正常铁调素表达;III类,膜铁转运蛋白的缺陷阻止铁调素的正常调节。
总结
铁调素-铁转运蛋白相互作用,以维持稳定的体内铁含量和血浆铁浓度。如果平衡被打破,则是一系列铁疾病的发病机制的基础,因此,血浆铁调素浓度测定与铁其他相关参数指标结合可用于诊断铁紊乱。
【参考文献】
[1]Georgieff MK, Krebs NF, Cusick SE. The Benefits and Risks of Iron Supplementation in Pregnancy and Childhood. Annu Rev Nutr. 2019 Aug 21;39:121-146.
[2]Nancy C. Andrews; Forging a field: the golden age of iron biology. Blood 2008; 112 (2): 219–230.
[3]Nemeth E, Ganz T. Hepcidin-Ferroportin Interaction Controls Systemic Iron Homeostasis. Int J Mol Sci. 2021 Jun 17;22(12):6493.
[4]Tomas Ganz, Gordana Olbina, Domenico Girelli, Elizabeta Nemeth, Mark Westerman; Immunoassay for human serum hepcidin. Blood 2008; 112 (10): 4292–4297.
