患者手足抽搐,竟与这种胃炎有关!
2026-03-27 15:18 文章来源:
作者:佘秋民
单位:深圳市宝安区松岗人民医院
2026 年1月1日下午,在审核一份报告时,发现 α- 羟丁酸脱氢酶(HBDH)高达 752 U/L。第一反应怀疑该标本是否溶血,立即查看,血清颜色正常;接着查看该项目的反应曲线,检测区间的吸光度变化呈线性;最后查看 HBDH 当日质控,均在控,基本排除结果检测误差。查看该患者相关结果,血常规结果如下图:
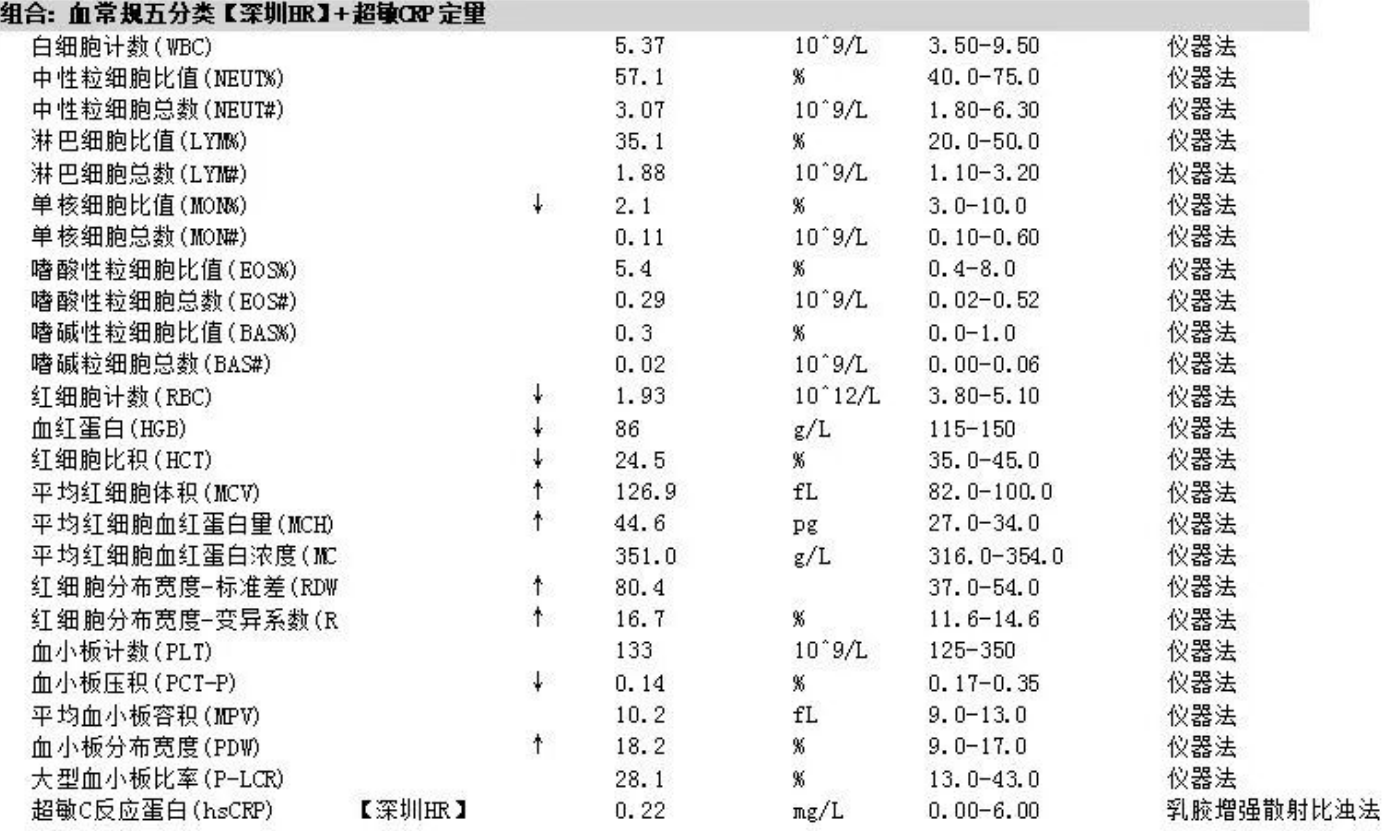
结合 MCV、MCH、MCHC、RDW-CV,考虑大红细胞不均匀性贫血。因 WBC、PLT 均正常,首要考虑为巨幼细胞性贫血导致 HBDH 异常升高,随即查阅该患者病史如下:
患者女,46 岁。主诉:手足抽搐 2 天;现病史:间歇出现手指抽动,无肢体麻木、疼痛;既往史、个人史、家族史:无特殊;过敏史:未发现
体格检查:血压 118/76 mmHg;神清,双肺呼吸音清,未闻及干湿性啰音;心率 75 次 / 分,律齐,各瓣膜听诊区未闻及杂音;腹平软,无压痛、反跳痛;双下肢无水肿。辅助检查:暂缺。
诊断:手足搐搦。
结合其他生化指标:Ca 2.26 mmol/L,GLU 6.16 mmol/L,基本可排除低钙血症所致手足搐搦及糖尿病所致周围神经病变。鉴于巨幼细胞性贫血由叶酸和(或)维生素 B12 缺乏引起,立即加做贫血三项(叶酸、维生素 B12、血清铁蛋白),结果如下:
至此,真相似乎已尘埃落定,诊断为维生素B12缺乏引起的巨幼细胞性贫血。
维生素B12或叶酸缺乏导致骨髓中的造血前体细胞(幼红细胞)在发育早期就死亡(即无效造血),大量的巨幼红细胞在骨髓内破裂、凋亡时,将其内容物LDH释放入血,导致LDH和HBDH升高【HBDH 是 LDH 活性的一部分,主要代表 LDH 同工酶中 LDH-1 和 LDH-2 的活性】。缺乏维生素B12会导致神经纤维的髓鞘受损,神经信号传导紊乱,引起神经肌肉兴奋性增高和运动控制障碍,表现为肌肉震颤、手足搐搦(抽动)、腱反射亢进或病理征阳性。
回顾本案例,脑海中突然有一个疑问,是什么原因导致这名中年女性缺乏维生素B12呢?我们知道,导致维生素B12缺乏的主要原因包括长期素食引起的摄入不足;胃肠道疾病或术后引起的吸收障碍;某些长期服用的药物如质子泵抑制剂,H2受体阻滞剂,二甲双胍等会干扰维生素B12的吸收或代谢以及A型胃炎(自身免疫性胃炎)由于产生了针对壁细胞(分泌胃酸和内因子)和内因子的自身抗体导致维生素B12无法吸收。
随后,电话联系了患者,获悉平时为正常饮食,未服用任何药物,胃肠情况良好,综合分析,难道是产生了抗壁细胞抗体或抗内因子抗体导致的维生素B12缺乏,遂将该标本外送做了内因子抗体检测,结果如下:
至此,真相大白,该患者是一名由于A型胃炎引起维生素B12缺乏,导致恶性贫血和神经系统症状出现的案例。
本案例始于一份异常的HBDH,终于一例A型胃炎的诊断,检验思维贯穿全程:
1.HBDH升高 ≠ 心脏损伤:遇到HBDH单独显著升高,尤其无心肌酶谱同步异常时,应警惕血液系统疾病(尤其是巨幼细胞性贫血的无效造血)。这是检验与临床沟通的重要切入点。
2.血常规是“导航图”:大细胞性贫血(MCV升高)+ 红细胞大小不均(RDW-CV升高),是提示维生素B12/叶酸缺乏的经典信号。当生化指标与血常规矛盾时,务必交叉验证。
3.病因深挖:不止于“缺啥补啥”:本例维生素B12缺乏确诊后,并未止步。通过排除摄入不足、药物等因素,最终以抗内因子抗体阳性锁定A型胃炎。这提示:遇到无法解释的维生素B12缺乏,应建议临床追查吸收障碍的根源(自身免疫、胃肠病变等)。
4.检验指标是“侦察兵”:从HBDH到MCV,再到维生素B12和抗体,检验指标构成了完整的证据链。主动分析、主动追问,是检验从“辅助”走向“临床决策支持”的关键。
A型胃炎致维生素B12缺乏的病理生理机制及临床表现。
1. 自身免疫性损伤:核心病因
A型胃炎(自身免疫性胃炎)的本质是T细胞介导的胃黏膜慢性炎症。机体产生针对壁细胞及其成分的自身抗体(抗壁细胞抗体和抗内因子抗体),导致胃体(主要涉及胃底和胃体)黏膜萎缩,壁细胞选择性破坏。
2. 分子机制:内因子缺乏与维生素B12吸收障碍
内因子缺失:壁细胞丧失直接导致内因子分泌急剧减少。内因子是回肠末端吸收维生素B12所必需的转运蛋白。
吸收阻断:饮食中的维生素B12(与蛋白质结合)虽可在胃酸和蛋白酶作用下释放,但因缺乏内因子,无法形成“B12-内因子复合物”,导致其无法与回肠黏膜刷状缘上的受体(cubilin受体)结合,最终随粪便排出,引发负平衡。
3. 细胞生化机制:维生素B12依赖性酶反应受阻
维生素B12(钴胺素)在体内作为两种关键酶的辅酶:
甲硫氨酸合成酶:催化同型半胱氨酸甲基化为甲硫氨酸,同时使5-甲基四氢叶酸脱甲基生成四氢叶酸。此途径受阻导致:DNA合成障碍:四氢叶酸再生减少,影响胸腺嘧啶核苷合成,导致DNA复制延缓,骨髓红系祖细胞发生巨幼样变(核炎性发育失衡)。
甲基化反应受损:甲硫氨酸减少影响S-腺苷甲硫氨酸的生成,干扰髓鞘基础蛋白的甲基化。
L-甲基丙二酰辅酶A变位酶:催化甲基丙二酰辅酶A转化为琥珀酰辅酶A。此途径受阻导致甲基丙二酸及其前体堆积,进而合成非生理性的异常支链脂肪酸。这些异常脂肪酸掺入神经髓鞘的脂质结构,破坏髓鞘的完整性(脱髓鞘改变)。
1. 血液系统:恶性贫血(巨幼细胞性贫血)
【症状】
隐匿起病,表现为乏力、苍白、头晕、活动后心悸(贫血);可伴有出血倾向(血小板减少)及感染风险增加(粒细胞减少)。
【机制】
DNA合成障碍导致骨髓三系细胞(红系、粒系、巨核系)成熟障碍,以红系最显著。骨髓呈巨幼红细胞增生,外周血可见卵圆形大红细胞(MCV升高)、中性粒细胞分叶过多。由于维生素B12缺乏同时影响叶酸代谢,故其贫血本质是核分裂障碍所致“无效造血”。
2. 神经系统:亚急性联合变性
【症状】
感觉性共济失调:步态不稳、踩棉花感、Romberg征阳性(闭眼站立不稳),震动觉和位置觉丧失。
周围神经病变:对称性肢体远端麻木、刺痛或烧灼感。
锥体束征:下肢无力、僵硬、痉挛,腱反射亢进,病理征阳性。
精神/认知症状:记忆力减退、易激惹、抑郁,严重者可出现痴呆。
【机制】
髓鞘脱失:异常脂肪酸掺入髓鞘导致轴索变性,首先累及脊髓后索(薄束、楔束,传递本体感觉),其次为侧索(皮质脊髓束,传递运动指令),同时累及周围神经。
轴索运输障碍:B12缺乏干扰轴浆运输,加重神经功能障碍。病变呈向心性发展,早期髓鞘肿胀、断裂,晚期轴索变性不可逆。
3. 消化系统及其他
【症状】早期可无明显消化道症状,部分患者出现腹胀、食欲减退。由于胃酸缺乏,可伴有高胃泌素血症,刺激胃肠嗜铬样细胞增生,增加发生I型胃神经内分泌肿瘤的风险,胃腺癌风险亦有所增高。
血清学:维生素B12水平降低;抗内因子抗体(特异性高,阳性即可确诊恶性贫血);抗壁细胞抗体(敏感但不特异)。
生化指标:胃泌素-17水平显著升高(因胃酸缺乏失去负反馈抑制);胃蛋白酶原I/II比值降低(反映胃体萎缩)。
血液学:MCV增高,血红蛋白降低,外周血涂片可见大卵圆形红细胞和中性粒细胞分叶过多。
维生素B12替代治疗:因吸收障碍,需肠外给药(肌注)。初始阶段大剂量补充以恢复储存,随后终身维持治疗(通常每月一次)。早期神经症状可逆,晚期轴索损伤常遗留后遗症。
内镜监测:因胃黏膜萎缩存在恶变潜能,需定期胃镜随访。
