血小板进行性降低之谜
2024-01-18 11:24 文章来源:
作者:刘亚如
单位:南京同仁医院
患者女性,79岁,因腰背疼痛1周,加重伴全身无力2天入院,拟“乏力待查”收入院。既往有2型糖尿病,高血压病史,有脑梗死病史,长期口服阿托伐他汀片调脂稳斑、氯吡格雷抗凝。
案例分析
一、检查结果
实验室检查
该患者12月8号血常规检查中PLT:22x109,结果为危急值,触碰复检规则。查看标本无凝块,镜检符合,查历史结果发现血小板进行性的下降。
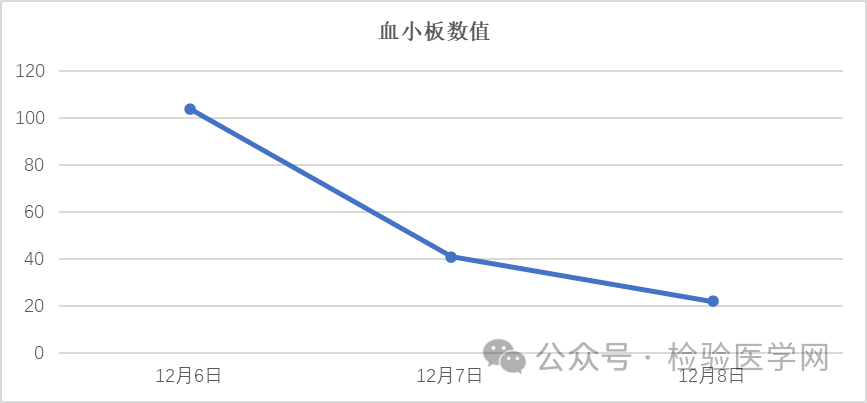
图1 血小板数值
查看患者其他结果如图2、图3所示。

图2 凝血结果
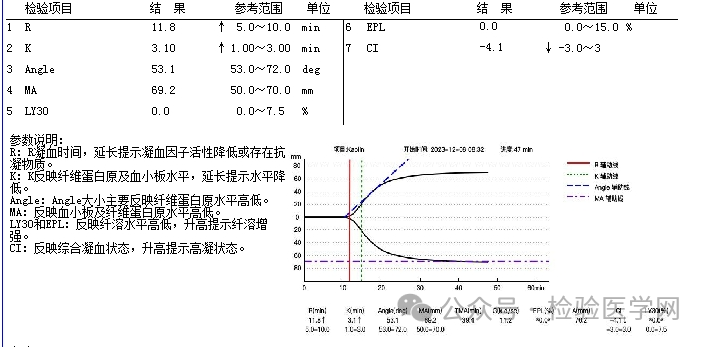
图3 12月8日血栓弹力图
R延长提示凝血因子缺乏,但是APTT正常,查看病例患者12月7日曾注射低分子肝素。MA是凝血酶激活的血小板的功能,主要反应血小板和纤维蛋白原的功能,虽然血小板比较低,但是纤维蛋白原高,所以MA表现正常。D-二聚体、FDP明显增高,凝血激活和继发纤溶,有肝素的用药史,血小板进行性的降低难道是HIT或DIC?
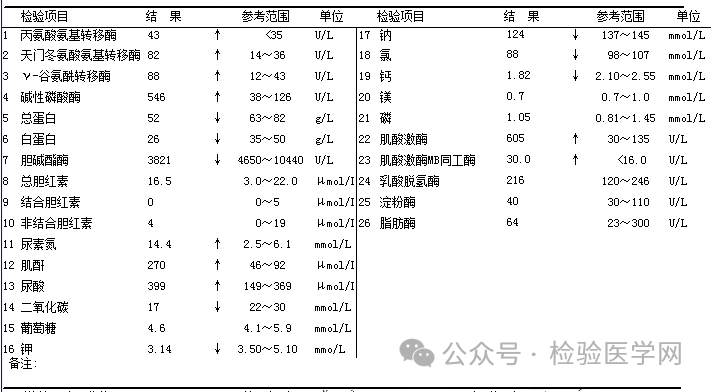
图4 生化结果
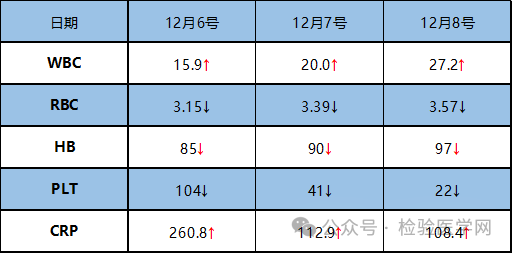
图5 血常规结果


图6 炎症指标
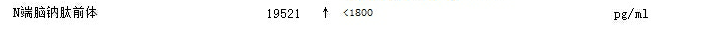
图7 心肌损伤标志
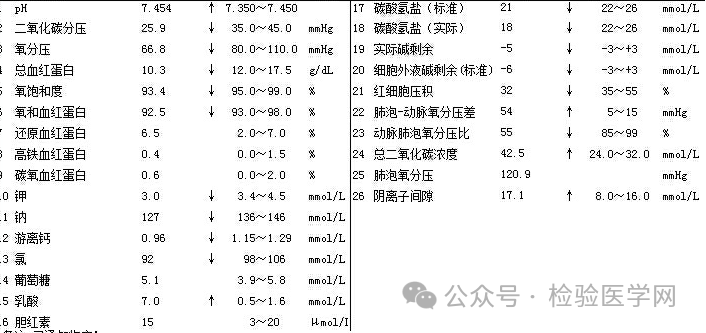
图8 血气结果
超声检查
右侧下肢动脉粥样硬化(斑块形成),右侧下肢深静脉管腔通畅;左侧下肢动脉粥样硬化(斑块形成),左侧下肢深静脉管腔通畅。
二、鉴别诊断
1、HIT:肝素诱导的血小板减少是由于血小板释放的PF4与肝素1:1结合后发生构象改变,刺激免疫细胞产生HIT抗体,HIT抗体与PF4-H结合形成大分子复合物,大量结合在血小板受体上,引起血小板持续活化形成微血栓及血小板数量减低。根据4T′S评分。
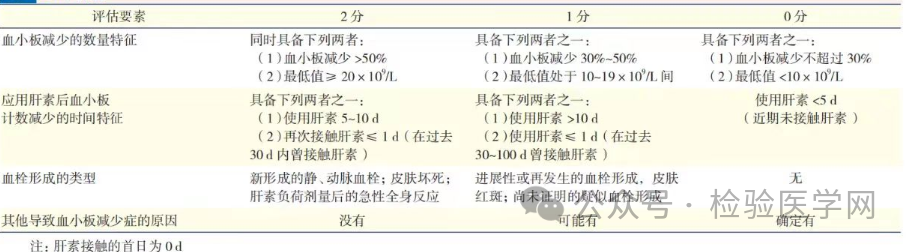
图9 4T′S评分
从凝血结果和血小板降低及DIC评分分析,该患者符合DIC特征。
患者是12月6号入院,肝素用药史小于5天,暂不考虑HIT。
2、TTP:是由于ADAMTS-13的活性明显下降,大分子量vWF多聚体诱导血小板活化和聚集,在末梢动脉、毛细血管内形成广泛的微血栓,导致血小板消耗性减低。从现有的检查结果来看间接胆红素、LDH、网织红细胞结果正常,外周血涂片未见裂片红细胞,暂不支持TTP。
3、DIC:各种原因导致凝血因子大量消耗形成微血栓,导致各器官功能障碍,后期激发纤溶亢进。经历高凝期、低凝期、纤溶亢进期。根据DIC评分。
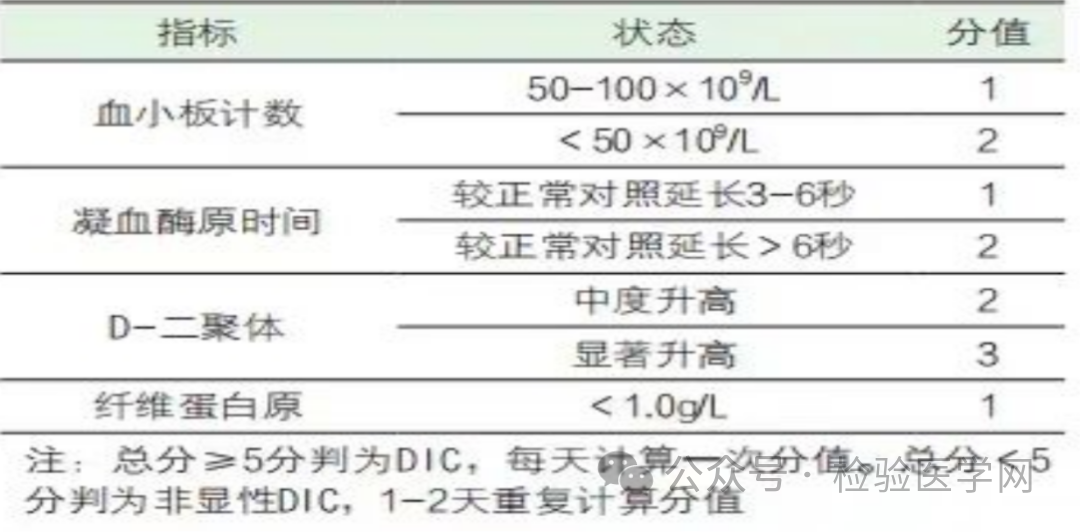
图10 DIC评分规则
4、炎症指标PCT>100.00ng/ml、IL-6>5000.00pg/ml、CRP 260.8mg/l显著升高,脓毒性特征明显。
脓毒症诊断标准:A)确诊感染或疑似感染。B)SOFA评分较基线增加>2分。
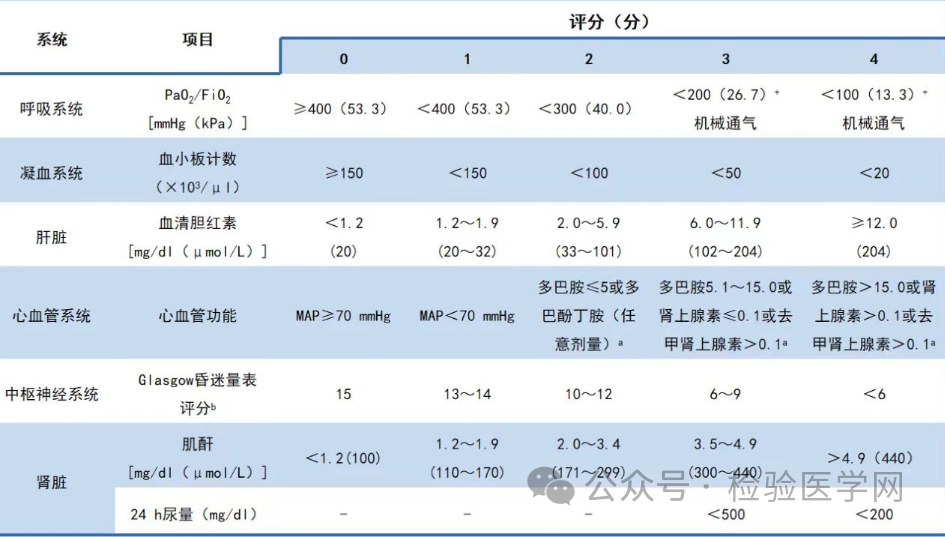
图11 SOFA评分规则
结合肝功能、肾功能、心肌等多器官功能障碍,心率快、血压低,支持脓毒性休克,血小板突然间降低是脓毒症引起DIC导致的。后续输注血小板,注射头孢哌酮钠舒巴坦钠抗炎,单次注射低分子肝素4100AXaI抗凝,予新活素静脉泵入改善心功能,味塞米静推利尿减轻心脏负荷,同时予多巴胺维持血压。患者血小板逐渐上升,炎症指标下降,反应迟钝较前好转,精神状态尚可。后续继续抗感染、补液、营养支持。
知识拓展
脓毒症导致血小板减少原因:
1、血小板生成减少,由于炎症感染导致骨髓受到抑制。
2、消耗增加,传统上血小板的激活是通过凝血酶介导的,在脓毒症中微生物的细胞特异性膜成分触发凝血,血小板和凝血因子不断消耗。
3、获得性嗜血细胞性淋巴细胞增多症,淋巴细胞的活化和增殖失调导致细胞因子过量产生。骨髓显示巨噬细胞活化伴嗜血细胞增多。
4、中性粒细胞外陷阱(NET):活化的血小板可以促进中性粒细胞募集到损伤部位,从而捕获并杀死病原体。NET为血栓提供框架和刺激。
5、血小板聚集/黏附到白细胞和内皮细胞上。
6、免疫性血小板减少,在30%-40%的脓毒症患者存在血小板相抗体[1]。血小板减少症(<50×109/L和50×109至99×109/L)显示疾病严重程度和死亡率增加,加重脓毒症期间部分受干扰的宿主反应[2]。血小板过度活化微血栓形成,导致多器官功能障碍,因此抑制血小板功能可以代表一种有用的减弱 炎症反应和改善结果。当前抗血小板药物 包括乙酰水杨酸、P2Y12抑制剂和GPIIb/IIIa拮抗剂,但是抗血小板药物对脓毒症患者结局的影响尚不清楚[3]。
脓毒症导致凝血紊乱:
在脓毒症中,中性粒细胞被激活,释放细胞外陷阱,这些陷阱由DNA、组蛋白和其他中性粒细胞颗粒蛋白组成,所有这些都是高度促血栓形成的,受损宿主细胞释放的损伤相关分子模式进一步增加了促血栓形成活性。受损血管内皮细胞通过表达组织因子和释放血管性血友病因子促进促血栓形成作用。脓毒症诱发的凝血功能障碍的治疗关键是快速及时地治疗潜在感染,抑制血栓形成,肝素和类肝素是多种血栓栓塞性疾病最常用的抗凝剂;然而,它们治疗脓毒症诱发的凝血病或DIC的有效性仍存在争议,通常仅限于预防深静脉血栓形成[4]。
【参考文献】
[1]. Vardon-Bounes F, Ruiz S, Gratacap MP, Garcia C, Payrastre B, Minville V. Platelets Are Critical Key Players in Sepsis. Int J Mol Sci. 2019 Jul 16;20(14):3494. doi: 10.3390/ijms20143494. PMID: 31315248; PMCID: PMC6679237.
[2]. Claushuis TA, van Vught LA, Scicluna BP, Wiewel MA, Klein Klouwenberg PM, Hoogendijk AJ, Ong DS, Cremer OL, Horn J, Franitza M, Toliat MR, Nürnberg P, Zwinderman AH, Bonten MJ, Schultz MJ, van der Poll T; Molecular Diagnosis and Risk Stratification of Sepsis Consortium. Thrombocytopenia is associated with a dysregulated host response in critically ill sepsis patients. Blood. 2016 Jun 16;127(24):3062-72. doi: 10.1182/blood-2015-11-680744. Epub 2016 Mar 8. PMID: 26956172.
[3]. Ouyang Y, Wang Y, Liu B, Ma X, Ding R. Effects of antiplatelet therapy on the mortality rate of patients with sepsis: A meta-analysis. J Crit Care. 2019 Apr;50:162-168. doi: 10.1016/j.jcrc.2018.12.004. Epub 2018 Dec 5. PMID: 30551047.
[4]. Iba T, Levy JH. Sepsis-induced Coagulopathy and Disseminated Intravascular Coagulation. Anesthesiology. 2020 May;132(5):1238-1245. doi: 10.1097/ALN.0000000000003122. PMID: 32044801
